云南组织pcr原理
PCR样本可分2种,DNA样本和RNA样本。一,DNA样本:已经提取好的DNA样本,负80度保存,干冰运输;血液样本,需全血,加入抗凝剂,抗凝管4度保存;组织样本,需冻存管或干净灭菌的离心管装,负80度保存,干冰运输;细胞样本,用胰酶消化后的细胞沉淀,负20度或负80度保存。二,RNA样本:提取好的RNA样本,负80度保存,干冰运输;血液样本,全血,加入抗凝剂,4度冰箱保存;组织样本,冻存管或干净灭菌离心管,负80度保存,干冰运输;细胞样本,用胰酶消化后的细胞沉淀,负20度或负80度保存。长时间保存,可加Trizol,其中血液用TrizolLS组织和细胞沉淀用Trizol。英瀚斯生物pcr检测,保证真实实验检测,数据保密完整性。云南组织pcr原理
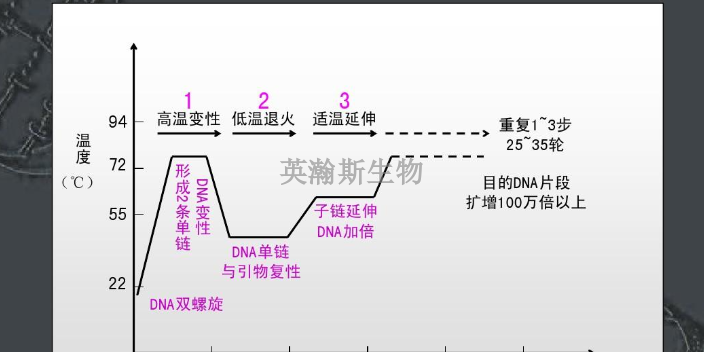
pcr是一种在体外扩增特定DNA序列的技术方法,通过与特定DNA区域两端互补的寡核苷酸为引物(primer)在试管中DNA聚合酶选择性地单独复制合成介于两引物直接的基因片段,如同DNA复制中的半保留复制一样,新合成的基因片段与模板链形成新的DNA双链,经反复的变性(denature)引物退火(anerling)和引物延伸(extention)三步循环,前一循环合成的DNA链成为下一循环引物结合的模板,每循环一次,反应体系的DNA的量就增加一倍,20-30次反复循环,即可由微量的DNA模板开始获得大量的DNA特异片段。近年来,PCR迅速发展,已深入生命科学的各个领域,技术方法不端完善,基本的PCR实验技术主要有经典PCR技术、RT-PCR技术、免疫-PCR技术、PCR-SSCP技术等。湖北靠谱pcr英瀚斯生物,可承接各类荧光定量pcr检测。
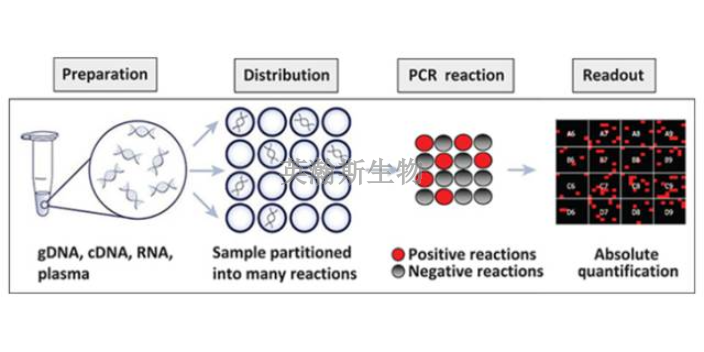
PCR出现假阳性的原因分析。引物设计不合适:选择的扩增序列与非目的扩增序列有同源性,因而在进行PCR扩增时,扩增出的PCR产物为非目的性的序列。靶序列太短或引物太短,容易出现假阳性。需重新设计引物。靶序列或扩增产物的交叉污染:这种污染有两种原因:一是整个基因组或大片段的交叉污染,导致假阳性。这种假阳性可用以下方法解决:①操作时应小心轻柔,防止将靶序列吸入加样器内或溅出离心管外。②除了酶及其他不耐高温的物质外,所有试剂或器材均应高压消毒。所用离心管均应一次性使用。③必要时,在加标本前,反应管和试剂用紫外线照射,以破坏存在的核酸。二是空气中的小片段核酸污染,这些小片段比靶序列短,但有一定的同源性。可互相拼接,与引物互补后,可扩增出PCR产物,而导致假阳性的产生,可用巢式PCR方法来减轻或消除。
原位PCR就是在组织细胞里进行PCR反应,它结合了具有细胞定位能力的原位杂交和高度特异敏感的PCR技术的优点,是细胞学科研与临床诊断领域里的一项有较大潜力的新技术。原位PCR是Hasse等于1990年建立的,实验用的标本是新鲜组织、石蜡包埋组织、脱落细胞、血细胞等。其基本方法为:1、固定组织或细胞:将组织细胞固定于预先用四氟乙烯包被的玻片上,并用多聚甲醛处理,再灭活除去细胞内源性过氧化物酶。2、蛋白酶K消化处理:用60ug/ml的蛋白酶K将固定好的组织细胞片55℃消化处理2h后,96℃2min以灭活蛋白酶K。3、PCR扩增:在组织细胞片上,加PCR反应液,覆盖并加液体石蜡后,直接放在扩增仪的金属板上,进行PCR循环扩增。有的基因扩增仪带有专门用于原位PCR的装置。4、杂交:PCR扩增结束后,用标记的寡核苷酸探针进行原位杂交。5、显微镜观察结果。pcr检测实验数据如何分析?
PCR实验技术中的Touch-downPCR介绍:Touch-downPCR又称降落PCR.即选定一个温度范围,如50—35℃,每降1-2℃进行1-2个循环,然后在50度下进行15个循环。Touch-down的原理随着退火温度的降低,特异性逐步降低,但特异性条带在温度较高时已经扩增出来,其浓度远远超过非特异性条带,随着退火温度的降低,特异性条带优先被扩增。选择初始复性温度的原则起始复性温度应该比引物的Tm值高出5-10度,然后每个循环递减1-2度Touch-downPCR的应用范围lowcopyoftargetedDNA;highdegreedegeneracy(orlessspecific)ofthefirstsetofprimers;荧光定量pcr正常值多少?安徽荧光定量pcr技术
pcr检测,**常规的实验,英瀚斯生物给您**靠谱的结果。云南组织pcr原理
PCR实验技术的发展历程,Khorana(1971)等**早提出核酸体外扩增的设想:“经DNA变性,与合适的引物杂交,用DNA聚合酶延伸引物,并不断重复该过程便可合成tRNA基因。”1983年4月的一个星期五晚上,他开车去乡下别墅的路上,猛然闪现出“多聚酶链式反应”的想法。1983年12月,Mullis用同位素标记法看到了10个循环后的49bp长度的***个PCR片段;1985年,KaryMullis在Cetus公司工作期间,发明了PCR。Mullis要合成DNA引物来进行测序工作,却常为没有足够多的模板DNA而烦恼。1985年10月25日申请了PCR的**,1987年7月28日批准(**号4,683,202),Mullis是发明人;1985年12月20日在Science杂志上发表了篇PCR的学术论文,Mullis是共同作者;1986年5月,Mullis在冷泉港实验室做专题报告,全世界从此开始学习PCR的方法云南组织pcr原理
南京英瀚斯生物科技有限公司坐落在南京市栖霞区燕子矶街道和燕路371号东南大学国家大学科技园科创楼A311,是一家专业的医学实验外包、动物实验外包、细胞实验外包、分子实验检测、病理染色检测、科研实验外包、动物模型构建、第三方检测、病理组织切片、细胞培养、电生理检测、医学研究和试验发展、生物医药技术研发、技术转让、技术咨询及技术服务公司。公司目前拥有专业的技术员工,为员工提供广阔的发展平台与成长空间,为客户提供高质的产品服务,深受员工与客户好评。公司以诚信为本,业务领域涵盖实验外包,动物模型构建,细胞分子实验,病理检测,我们本着对客户负责,对员工负责,更是对公司发展负责的态度,争取做到让每位客户满意。公司力求给客户提供全数良好服务,我们相信诚实正直、开拓进取地为公司发展做正确的事情,将为公司和个人带来共同的利益和进步。经过几年的发展,已成为实验外包,动物模型构建,细胞分子实验,病理检测行业出名企业。
- 溃疡性结肠炎动物模型造模方法 2025-08-01
- 动物肺动脉高压模型外包 2025-08-01
- 脑出血小鼠模型构建 2025-08-01
- asthma大鼠模型造模方法 2025-08-01
- 动物阴道炎模型造模方法 2025-08-01
- 动物HLP模型构建 2025-08-01
- 轻度脑损伤(mTBI)构建大鼠模型建立 2025-08-01
- asthma大鼠模型 2025-08-01
- 疼痛模型建立 2025-08-01
- 大鼠睡眠剥夺模型构建 2025-07-31
- 需求中盐核酸酶联系方式 2025-08-01
- 青海哪里有雅安藏茶销售电话 2025-08-01
- 全自动微机熔点仪品牌 2025-08-01
- 南通超微结构免疫电镜检测哪家专业 2025-08-01
- 宝山区切片服务费 2025-08-01
- 溃疡性结肠炎动物模型造模方法 2025-08-01
- 河南快速牙托粉 2025-08-01
- 宝山区推荐信息系统集成设计 2025-08-01
- 陕西哪些华壹唯维佳产品 2025-08-01
- 杭州甲萘醌-7生产公司 2025-08-01